组织粘合剂和止血剂是组织工程和伤口愈合的潜在替代方法,因此引起了广泛的关注。但是,这些粘合剂通常与紫外线引起的交联或化学反应有关,这可能导致受创组织的继发性损伤。此外,在伤口愈合过程中,粘合剂的缓慢降解会阻止运动细胞的迁移,并抑制细胞外基质微环境的重塑,从而阻碍伤口的愈合。此外,粘性水凝胶也得到了广泛的研究。例如,由银-木质素纳米微粒、丙烯酸和果胶组成的粘合剂水凝胶具有良好的粘接性能和高韧性,可以被用来修复皮肤缺陷。但是,粘性水凝胶在用于组织粘合时通常会发生溶胀,导致其力学性能急剧下降,进而引起伤口愈合过程中粘性水凝胶的破裂。而且,粘性水凝胶的溶胀可导致组织受压和严重的并发症。为应对新型粘合剂的持续需求,研究人员将注意力转向了自然界中的体系,例如贻贝分泌物。在这些材料中,多个超分子相互作用(包括静电作用,π-π键,氢键和范德华力)的相互作用造就了其出色的粘合性能。其他的体系主要集中在仿生小分子系统上,由于这类体系表现出的粘合能力都较弱,因此它们在生物医学应用方面受到了限制。目前为止,开发出能在外科应用中保持持久粘合性能的粘合剂仍然是一个挑战。
为了应对这一挑战,清华大学刘凯副教授团队创造性地开发了一种具有强大粘合性能的非溶胀性蛋白质粘合剂,主要用于水下和体内应用场景。这种材料依靠带有大量电荷的多肽(supercharged polypeptides,SUPs)与带相反电荷的仿生合成表面活性剂(包含3,4-二羟基苯丙氨酸或偶氮苯基团)之间的静电络合作用形成超强粘性凝聚层。而邻苯二酚基团和静电作用的协同作用使得该生物粘接剂具有非凡的粘合性能。这种新型的多肽改性凝聚层粘合剂有望在外科应用中替代现有的产品。

文章亮点:
1、所获得的凝聚层粘合剂具有优异的粘合性能,在铁离子的络合作用下,其与铁基底的粘合性能(粘接强度13.5 ± 1.6 MPa)优于目前市场上的氰基丙烯酸酯(粘接强度10.4 ± 0.6 MPa)。该粘合剂在水下环境中,其粘合能力(粘接强度~0.4 MPa)比其他已报道的基于蛋白质的粘合剂都要强。
2、在体内止血实验中,该粘合剂能在10s内抑制猪肝脏和肾脏的出血。同时,相比于水凝胶材料,表现出了优异的抗溶胀性能。
3、该粘合剂在小鼠伤口闭合实验中,显示出持久的粘合性能、出色的促进伤口密封与愈合的能力以及抵抗炎症的特性,在外科应用中具有广阔的前景。
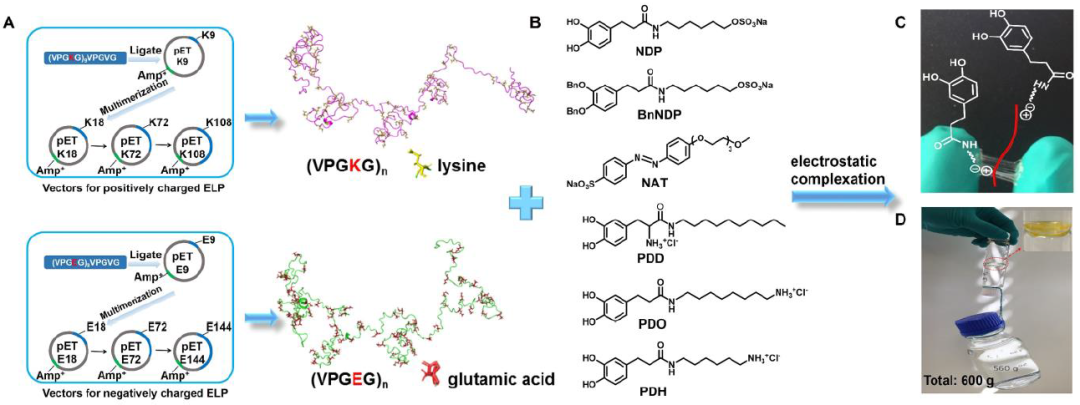
图1 SUP-表面活性剂凝胶层粘合剂的制备和表征
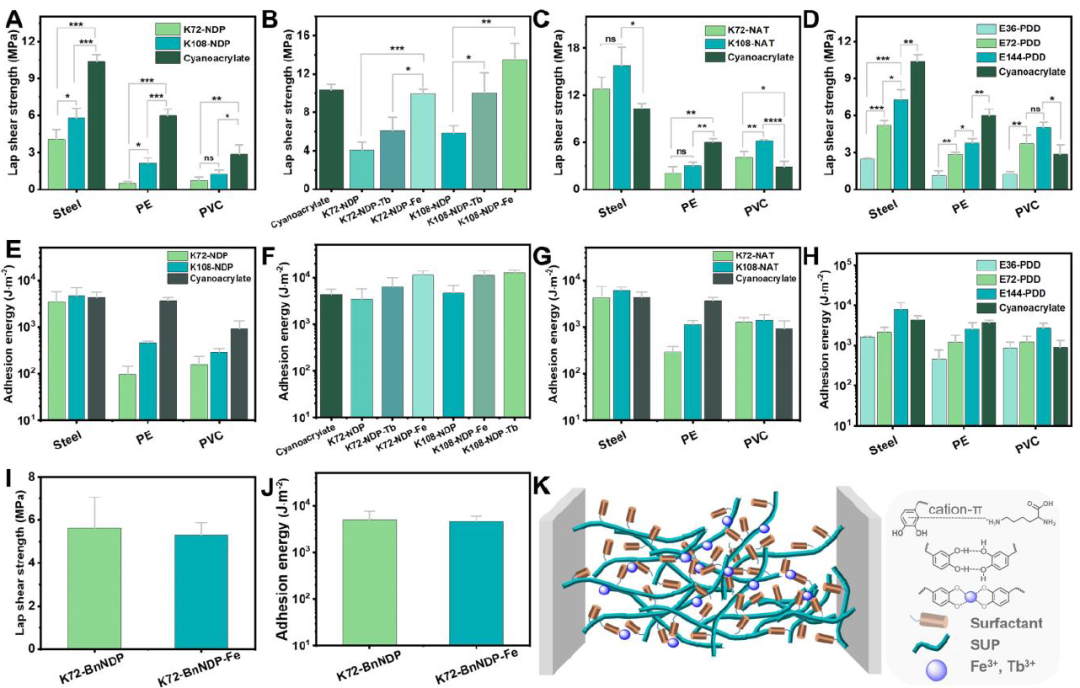
图2 SUP凝聚层粘合剂的粘合性能
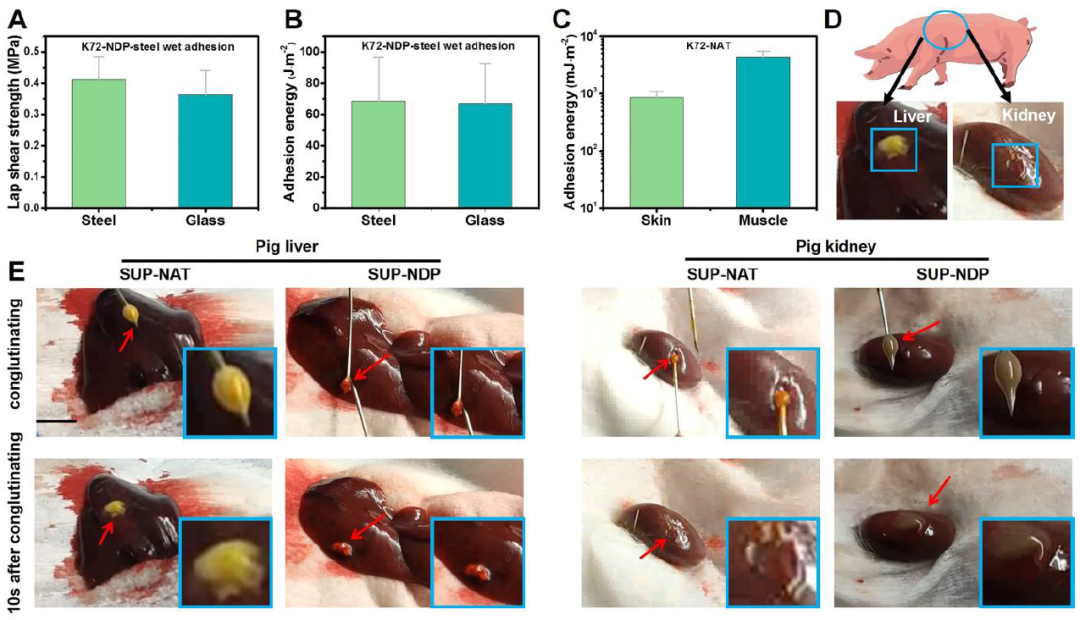
图3 SUP凝聚层粘合剂在体外实验和体内应用中的定量评估
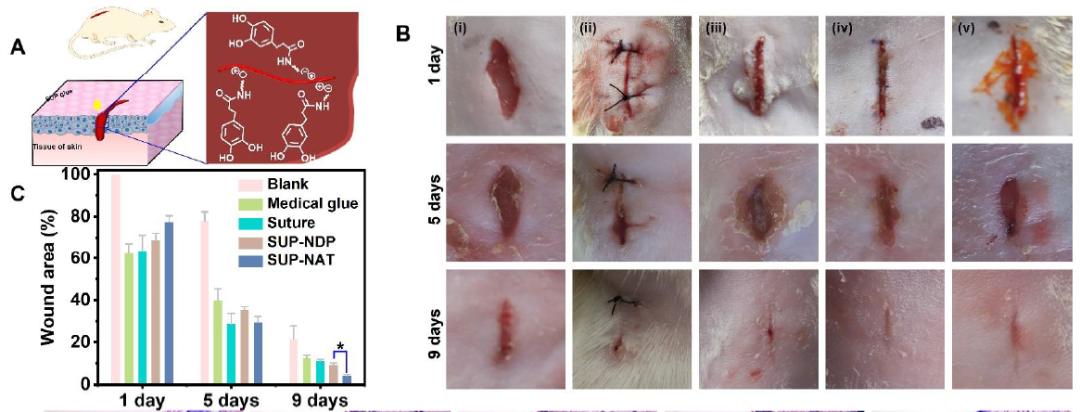
图4 用SUP粘合剂处理的小鼠伤口密封与愈合情况
全文链接:

发表评论