胰蛋白酶的发现
1846年,法国实验生理学家克劳德• 伯尔纳(ClaudeBernard,1813~1878)在开展兔子消化方式的研究,他注意到了一只食草的兔子(对,就是吃草的兔子!),它似乎是吃了其他的小动物,也许是鼠类(兔子窝边草都不吃呢,怎么会吃老鼠?),因为它竟然排出食肉动物才有的酸性而清澈的尿液。伯尔纳对兔子的消化方式非常感兴趣,于是解剖了兔子,仔细观察肉类在兔子胃中的消化状况,推理出胰腺与脂肪的吸收有关,酸性食物进入小肠将引起“胰液”分泌。但是由于当时研究的热点是巴普洛夫的反射学说,所以其后很长时间,没有引起人们的重视。
1876年,德国科学家威廉• 屈内(Wilhelm FriedrichKühne,1837~1900)在克劳德•伯尔纳的基础上,从“胰液”中分离提取出一种能降解其他生物物质的物质,它能降解其他的生物物质,这也是胰蛋白酶的第一次分离。他还发现胰蛋白酶最初是以胰蛋白酶原这一无活性的形式存在,经过转化成为活性胰蛋白酶。胰蛋白酶的发现使屈内成为第一位发现降解蛋白质的酶(即胰蛋白酶)的科学家,并且于1878年首次提出了酶(Enzyme)的概念。
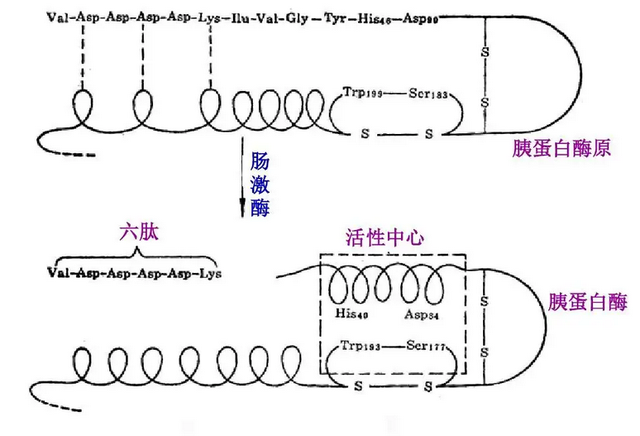
图1 胰蛋白酶原活化为胰蛋白酶
胰蛋白酶特点和应用
胰蛋白酶属于丝氨酸蛋白酶类,能特异性地作用于肽链Lys或Arg残基的羧基端[1]。在生理上参与了动物体内的新陈代谢、消化、凝血等功能的重要过程[2]。在细胞生物学领域,胰蛋白酶能使细胞膜与培养皿结合处蛋白降解,使得两者分离。并且由于细胞自身内部细胞骨架的张力以及培养液表面张力的作用下成为球形,从而实现细胞的消化。
其前体是没有活性的胰蛋白酶原,从胰腺分泌之后在小肠中被肠激酶或胰蛋白酶激活[3]。不过尴尬的是,胰蛋白酶本身也是蛋白质,所以厉害起来连自己都切,由原先的β-胰蛋白酶转化为α-胰蛋白酶,进一步降解为拟胰蛋白酶乃至碎片,活力也逐步下降而丧失。因此胰酶在制剂和活性、稳定性的平衡上,面临一些问题。
目前市面上的胰蛋白酶产品主要有冻干粉和液体两个形式。未改造的胰蛋白酶一般通过冻干的形式储存,复溶后使用,这样保证了酶的活性,使用中,Ca2+有保护和激活作用。为了满足液体制剂的需求,胰蛋白酶通常也会经过特殊处理消除乳糜蛋白酶活性和甲基化或者突变以防止自切。
这是重组胰蛋白酶的时代
早期的胰蛋白酶在生物制药的主要应用是胰岛素的生产,但很快也在其他领域发光发热。但是它的“出生”地——猪、牛、羊胰脏,给他带来了很多使用限制。动物来源的胰蛋白酶虽然来源广、价格低的,但这种动物来源的胰蛋白酶一直被生物界质疑,其安全性有一个致命缺点——携带大量可感染人的病毒,至少有67种之多[4]!因此,现代生物制药生产中动物源性原料使用具有潜在风险,一些人畜共患病毒都有可能被带入终产品中。如牛的BSE/TSE病毒,猪的口蹄疫病毒,人和动物之间传播的禽流感病毒等等。因此,动物来源胰蛋白酶产品受到严格的质量控制,但遗憾的是风险一直都在。
20世纪60年代曾在脊灰疫苗中曾检测到SV40病毒,在黄热减毒活疫苗中发现禽白血病病毒。2010年,又在轮状病毒疫苗中也先后检测到猪圆环病毒核酸(PCV)序列(Merck,GSK),当时推测“元凶”可能是增殖中所用的猪胰蛋白酶。
GMP生产规则和减少动物源性原辅料的使用,大大降低了外源因子污染的概率。政策层面,2019年9月国家药监局发布了《疫苗上市后生产工艺变更研究技术指导原则》(征求意见稿):“生产过程中,应尽可能避免使用人源或动物源性原材料”,疫苗生产原辅料变更,将动物源性的牛血清或胰酶变更为无动物源的原辅料,只需要通过简化变更流程,鼓励企业进行无动物源原辅料的变更。
美国2015年颁布重组胰蛋白酶标准,之后国外重组胰蛋白酶的应用开始增加。2020年版《中国药典》也增加了重组胰蛋白酶标准[5],将加快我国非动物源性生物药物的研发。
1974年,胰蛋白酶晶体结构被解析,并被归类为丝氨酸蛋白酶家族。20世纪80年代末90年代初,通过定点突变和重组胰蛋白酶,研究了胰蛋白酶特殊氨基酸位点的功能。此后重组胰蛋白酶生产开始出现,利用基因重组技术在重组大肠杆菌中生产胰蛋白酶,可以完美避开动物病毒污染的风险。重组胰蛋白酶从根源上对动物源胰蛋白酶进行了降维打击,我们也会在下一篇的文章中详细给大家讲讲胰蛋白酶的动物源与非动物源的差别。
当前,重组胰蛋白酶已逐渐成为更高标准、更高要求的生物制药首选。此外,部分疫苗批签发还增加胰酶残留检测项目。如此以来,企业势必也会倾向于使用安全性更加的重组胰蛋白,AOF生物药物的发展方向。
上海逐典自研的Trypelectase
非动物来源的重组胰蛋白酶
随着新颁布的2020年版《中国药典》首次增加了重组胰蛋白酶的标准。国内在生物制药生产使用安全性更高的重组胰酶已然是未来的趋势。

为此上海逐典推出了专为疫苗、病毒载体生产设计的Trypelectase重组胰蛋白酶,聚焦于提供高效、非动物源和高质量标准的产品。
该胰蛋白酶氨基酸序列与猪/牛胰腺来源的胰蛋白酶一致,由大肠杆菌 (E.coli)重组表达生产。非动物源、GMP级别、药典标准的Trypelectase重组胰蛋白酶真正做到在传统动物源胰蛋白酶基础上的更新换代!
产品特点
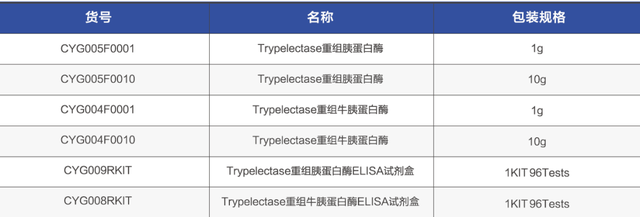
订购信息
来电咨询:李经理 18768160320
[1]lsen JV, Ong SE & Mann M. Trypsin cleaves exclusively C-terminalto arginine and lysine residues [J], Mol Cel Proteomics, 2004,3(6):608-614.
[2]Lopes AR, Juliano MA, Juliano L, et al. Coevolution of insecttrypsins and inhibitors [J], Arch Insect Biochem Physiol, 2004,55(3):140-152.
[3]Berdutina A V., Neklyudov A D., Ivankin A I, et al.. Comparison ofproteolytic activities of the enzyme complex from mammalian pancreasand pancreatin[J].Applied Biochemistry and Microbiology, 2000, 36(4):363-367.
[4]Marcus-Sekura C,RichardsonJC,HarstonRK,etal. Evaluation of the human host range of bovine and porcine virusesthat may contaminate bovine serum and porcine trypsin used in themanufacture of biological products[J].Biologicals,2011,39(6):359-369.
[5]《中国药典》2020年版, 重组胰蛋白酶

发表评论